
Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Cryptokokken meningitis
Medisch expert van het artikel
Laatst beoordeeld: 12.07.2025
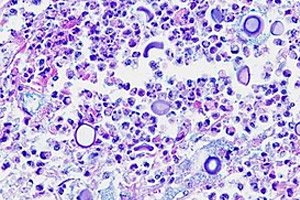
Ontsteking van de hersenvliezen kan niet alleen worden veroorzaakt door bacteriën, virussen en protisten, maar ook door schimmelinfecties. Cryptokokkenmeningitis wordt veroorzaakt door ingekapselde gistschimmels Cryptococcus neoformans, een opportunistische ziekteverwekker voor mensen. [ 1 ] De ziekte kreeg de naam Busse-Buschke-ziekte vanwege de eerste beschrijving door Otto Busse en Abraham Buschke in 1894. [ 2 ]
Volgens ICD-10 is de ziektecode G02.1 (in het gedeelte over ontstekingsziekten van het centrale zenuwstelsel), en ook B45.1 in het gedeelte over mycosen (dat wil zeggen schimmelziekten).
Epidemiologie
Acht van de tien gevallen van cryptokokkenmeningitis komen voor bij mensen die besmet zijn met HIV/AIDS.
Volgens gegevens gepubliceerd in The Lancet Infectious Diseases in het voorjaar van 2017, veroorzaakt de schimmel jaarlijks ongeveer 220.000 gevallen van cryptokokkenmeningitis bij mensen met hiv of aids, en sterven er meer dan 180.000 mensen aan. De meeste gevallen van cryptokokkenmeningitis komen voor in Sub-Sahara Afrika.
Volgens statistieken van de WHO werden in 2017 in Afrika 165,8 duizend gevallen van cryptokokkenmeningitis geregistreerd, 43,2 duizend in Aziatische landen, 9,7 duizend in Noord- en Zuid-Amerika en 4,4 duizend gevallen van de ziekte in Europese landen.
Oorzaken cryptokokkenmeningitis
De oorzaken van dit type meningitis zijn infectie met de schimmel Cryptococcus neoformans (klasse Tremellomycetes, geslacht Filobasidiella), die in de omgeving leeft: in de grond (inclusief stof), op rottend hout, in de uitwerpselen van vogels (duiven) en vleermuizen, enz. Infectie vindt plaats via de lucht - door het inademen van aerosol basidiosporen van de schimmel, hoewel bij de meeste mensen met voldoende immuniteit tegen de ontwikkeling van de ziekte, C. neoformans niet leidt en een facultatief intracellulair opportunistisch micro-organisme blijft (dat andere mensen niet kan infecteren). Lees ook - Cryptokokken - verwekkers van cryptokokkose [ 3 ]
Cryptokokkenmeningitis ontwikkelt zich in de regel bij HIV-geïnfecteerde personen (in stadium IVB) – als een secundaire infectie, maar ook bij mensen met een slecht functionerend immuunsysteem bij andere ziekten, gepaard gaand met langdurige immunosuppressie. [ 4 ]
Cryptokokkenmeningitis wordt beschouwd als een cerebrale of extrapulmonale vorm van cryptokokkose, die zich ontwikkelt na hematogene verspreiding van C. neoformans vanuit de luchtwegen en de longen naar de hersenen en het ruggenmerg.[ 5 ]
Risicofactoren
De factoren die het risico op het ontwikkelen van cryptokokkenmeningitis vergroten, zijn onder meer:
- neonatale periode (pasgeboren periode) en vroeggeboorte van zuigelingen;
- verzwakking van het immuunsysteem bij oncologische ziekten (waaronder leukemie, multipel melanoom, lymfosarcoom), bij patiënten met HIV-infectie en AIDS;
- suikerziekte;
- virale hepatitis en andere ziekten van het immuunsysteem;
- sikkelcelanemie;
- chemotherapie bij aanwezigheid van een oncologische diagnose;
- het overschrijden van het toegestane niveau van ioniserende straling;
- langdurige kuren met antibiotica of steroïden;
- plaatsing van intravasculaire katheters en shunts;
- beenmergtransplantatie of orgaantransplantatie.
Pathogenese
Cryptokokken, beschermd tegen menselijke immuuncellen door een polysaccharidecapsule (die fagocytose remt), scheiden proteasen, urease, fosfolipase en nuclease af – enzymen die in staat zijn gastcellen te vernietigen. [ 6 ]
En de pathogenese van cryptokokkose ligt in het feit dat deze enzymen cellen beschadigen door membranen te lyseren, moleculen te modificeren, de functies van celorganellen te verstoren en het cytoskelet te veranderen. [ 7 ]
Schimmelserineproteasen vernietigen de peptidebindingen van cellulaire eiwitten, splitsen immunoglobulinen en eiwitten van immuun-effectorcellen, en de replicatie van C. neoformans vindt plaats in mononucleaire fagocyten (macrofagen), wat hun verspreiding vergemakkelijkt. [ 8 ]
Bovendien verstoren cryptokokken, door endotheelcellen te passeren en door geïnfecteerde macrofagen binnen te dringen, de integriteit van de bloed-hersenbarrière (BBB). De schimmel verspreidt zich via de bloedbaan naar het hersenvocht en vervolgens naar de zachte membranen van de hersenen, waar hij in het hersenweefsel ‘kolonies’ van schimmelcellen vormt in de vorm van gelatineuze pseudocysten. [ 9 ]
Symptomen cryptokokkenmeningitis
De eerste tekenen van cryptokokkenmeningitis zijn koorts (temperatuur stijgt tot +38,5-39°C) en ernstige hoofdpijn.
Klinische symptomen omvatten ook misselijkheid en braken, toevallen, stijfheid van de nek, verhoogde gevoeligheid van de ogen voor licht en stoornissen in het bewustzijn en gedrag. [ 10 ]
Volgens deskundigen verloopt de ontwikkeling van het meningeaal syndroom langzamer dan bij een bacteriële infectie van de hersenvliezen.
Complicaties en gevolgen
Complicaties en gevolgen van schimmelmeningitis veroorzaakt door cryptococcus zijn:
- aanzienlijke stijging van de intracraniale druk;
- geïsoleerde schade aan de hersenzenuwen met parese/verlamming van de aangezichtszenuw en atrofische veranderingen in de oogzenuw (leidend tot oogheelkundige problemen);
- de uitbreiding van het ontstekingsproces naar de weefsels van de subcortex en de hemisferen van de hersenen - cryptokokkenmeningo-encefalitis;
- ontwikkeling van een hersenabces (cryptokokken);
- effusie in de subdurale ruimte (onder de dura mater van de hersenen);
- letsel aan het ruggenmerg;
- mentale veranderingen en verminderde cognitieve functies.
Diagnostics cryptokokkenmeningitis
Naast de medische voorgeschiedenis en het lichamelijk onderzoek, omvat de diagnose van een C. neoformans-infectie bij meningitis noodzakelijkerwijs bloedonderzoek: algemeen klinisch en biochemisch onderzoek, bloedserumanalyse op antilichamen tegen C. neoformans-eiwitten en bloedkweek.
Er wordt een lumbaalpunctie uitgevoerd en er wordt een analyse van het hersenvocht op antigeen uitgevoerd en er wordt een bacterioscopische analyse (bacteriekweek) van het hersenvocht gedaan. [ 11 ]
Instrumentele diagnostiek wordt uitgevoerd met behulp van röntgenfoto's van de borstkas en magnetische resonantie beeldvorming (MRI) van de hersenen.
Differentiële diagnose
De differentiële diagnose omvat meningitis en meningoencephalitis van bacteriële en virale oorsprong, hersenbeschadiging door schimmels Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis of amoeben (waaronder Naegleria fowleri).
Behandeling cryptokokkenmeningitis
De etiologische behandeling is gericht op het uitroeien van cryptokokken. Hiervoor worden antischimmelmiddelen gebruikt.
Het behandelingsregime omvat intraveneuze toediening (infuus, via een centraal veneuze katheter of via peritoneale infusie) van het polyene antischimmel antibioticum amfotericine B (Amphocyl) in combinatie met het antischimmelmiddel flucytosine (5-fluorocytosine) of fluconazol, dat een fungicide en fungistatische werking heeft. De dosering van deze geneesmiddelen wordt berekend op basis van het lichaamsgewicht van de patiënt.
Continue controle van de toestand van de patiënt is noodzakelijk, omdat Amfotericine B een toxisch effect heeft op de nieren. De bijwerkingen van Flucytosine kunnen bestaan uit onderdrukking van de hematopoëtische functie van het beenmerg, ademhalings- of hartstilstand, de ontwikkeling van huidletsels in de vorm van epidermale necrolyse, enz.
Volgens de aanbevelingen gepubliceerd in de update van de IDSA (Infectious Diseases Society of America) uit 2010 is de behandeling de afgelopen tien jaar niet veranderd. De eerstelijns antimycotische behandeling is gebaseerd op inductie, consolidatie en onderhoud van de volgende drie typen patiënten: [ 12 ]
HIV-gerelateerde ziekten
- Inductietherapie
- Amfotericine B-deoxycholaat (0,7-1,0 mg/kg/dag) + flucytosine (100 mg/kg/dag oraal) gedurende 2 weken (Bewijs A1)
- Liposomale amfotericine B (3-4 mg/kg/dag) of lipidecomplex amfotericine B (5 mg/kg/dag; nierfunctie controleren) + flucytosine (100 mg/kg/dag) gedurende 2 weken (Bewijs B2)
- Amfotericine B-deoxycholaat (0,7 tot 1,0 mg/kg/dag) of liposomaal amfotericine B (3 tot 4 mg/kg/dag) of amfotericine B-lipidencomplex (5 mg/kg/dag, voor patiënten die flucytosine niet kunnen verdragen) gedurende 4 tot 6 weken (Bewijs B2)
- Alternatieven voor inductietherapie
- Amfotericine B-deoxycholaat + fluconazol (Bewijs B1)
- Fluconazol + flucytosine (Bewijs B2)
- Fluconazol (Bewijs B2)
- Itraconazol (Bewijs C2)
- Fluconazol (400 mg/dag) gedurende 8 weken (gegevens A1)
- Fluconazol (200 mg/dag) gedurende 1 of meer jaar (Bewijs A1)
- Itraconazol (400 mg/dag) gedurende 1 of meer jaar (Bewijs C1)
- Amfotericine B-deoxycholaat (1 mg/kg/week) gedurende 1 of meer jaar (Bewijs C1)
- Consolidatietherapie
- Ondersteunende therapie
- Alternatieven voor onderhoudstherapie
Transplantatiegerelateerde ziekten
- Inductietherapie
- Liposomale amfotericine B (3-4 mg/kg/dag) of lipidecomplex amfotericine B (5 mg/kg/dag) + flucytosine (100 mg/kg/dag) gedurende 2 weken (Bewijs B3)
- Alternatieven voor inductietherapie
- Liposomale amfotericine B (6 mg/kg/dag) of lipidecomplex amfotericine B (5 mg/kg/dag) gedurende 4-6 weken (Bewijs B3)
- Amfotericine B-deoxycholaat (0,7 mg/kg/dag) gedurende 4-6 weken (Bewijs B3)
- Fluconazol (400 tot 800 mg/dag) gedurende 8 weken (Bewijs B3)
- Fluconazol (200 tot 400 mg/dag) gedurende 6 maanden tot 1 jaar (Bewijs B3)
- Consolidatietherapie
- Ondersteunende therapie
Niet-HIV/transplantatiegerelateerde ziekte
- Inductietherapie
- Amfotericine B-deoxycholaat (0,7 tot 1,0 mg/kg/dag) + flucytosine (100 mg/kg/dag) gedurende 4 of meer weken (Bewijs B2)
- Amfotericine B-deoxycholaat (0,7–1,0 mg/kg/dag) gedurende 6 weken (Bewijs B2)
- Liposomale amfotericine B (3-4 mg/kg/dag) of lipidecomplex amfotericine B (5 mg/kg/dag) in combinatie met flucytosine, 4 weken (Bewijs B3)
- Amfotericine B-deoxycholaat (0,7 mg/kg/dag) + flucytosine (100 mg/kg/dag) gedurende 2 weken (Bewijs B2)
- Consolidatietherapie
- Fluconazol (400 tot 800 mg/dag) gedurende 8 weken (Bewijs B3)
- Fluconazol (200 mg/dag) gedurende 6-12 maanden (Bewijs B3)
- Ondersteunende therapie
De combinatie van amfotericine B en flucytosine is bewezen het meest effectief te zijn in het elimineren van de infectie en heeft een groter overlevingsvoordeel laten zien dan amfotericine alleen. Vanwege de kosten is flucytosine echter vaak niet beschikbaar in gebieden met beperkte middelen waar de ziektelast hoog is. Combinaties van amfotericine B en fluconazol zijn onderzocht en hebben betere resultaten laten zien in vergelijking met amfotericine B alleen.[ 13 ], [ 14 ], [ 15 ]
Zonder behandeling leidt de ziekte tot verwardheid, toevallen, een lager bewustzijnsniveau en coma.
Hoofdpijn die ongevoelig is voor pijnstillers kan worden behandeld met spinale decompressie na adequate neuroimaging-evaluatie met CT of MRI. Het veilige maximale volume hersenvocht dat met één lumbaalpunctie kan worden gedraineerd, is onduidelijk, maar er wordt vaak tot 30 ml verwijderd met drukcontrole na elke 10 ml. [ 16 ]
Het voorkomen
Preventie van infectie met de schimmel Cryptococcus neoformans is in de eerste plaats noodzakelijk in gevallen van een zwak immuunsysteem. [ 17 ] Het wordt aanbevolen om stoffige plaatsen en het werken met aarde te vermijden, en HIV-geïnfecteerde mensen moeten voortdurend antiretrovirale therapie krijgen.
Prognose
Zonder behandeling is de prognose voor schimmelmeningitis slecht.
De eerste prognose hangt af van voorspellers van sterfte, zoals de volgende [ 18 ], [ 19 ]:
- De openingsdruk van het hersenvocht bedraagt meer dan 25 cm H2O.
- Laag aantal witte bloedcellen in hersenvocht
- Zintuiglijke beperking
- Late diagnose
- Verhoogde cerebrospinale vloeistof antigeentiters
- Snelheid van infectieverwijdering
- De hoeveelheid gist in het hersenvocht bedraagt meer dan 10 mm3 ( gebruikelijke praktijk in Brazilië) [ 20 ]
- Niet-HIV-gerelateerde patiënten en prognostische factoren bij deze patiënten, naast de reeds genoemde:
- Markers van een zwakke ontstekingsreactie
- Geen hoofdpijn
- Primaire hematologische maligniteit
- Chronische nier- of leverziekte
De sterfte varieert van land tot land, afhankelijk van de beschikbare middelen. In de Verenigde Staten en Frankrijk blijft de sterfte hoog, met sterftecijfers binnen 10 weken variërend van 15% tot 26%, en zelfs hoger bij niet-hiv-geïnfecteerde patiënten vanwege late diagnose en disfunctionele immuunreacties. Aan de andere kant stijgt de sterfte in landen met beperkte middelen van 30% tot 70% binnen 10 weken als gevolg van late presentatie en gebrek aan toegang tot medicijnen, bloeddrukmeters en optimale monitoring.

