
Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Door FDA goedgekeurd TIVDAK®: Tegen weefselfactor bij baarmoederhalskanker
Laatst beoordeeld: 02.07.2025
Op 29 april 2024 verleende de Amerikaanse Food and Drug Administration (FDA) volledige goedkeuring aan TIVDAK® (tisotumab vedotin) van Seagen Inc., een geneesmiddel gericht op weefselfactor (TF), voor de behandeling van patiënten met recidiverende of gemetastaseerde baarmoederhalskanker die tijdens of nachemotherapie is geprogresseerd. Dit is een belangrijke doorbraak in de behandeling van baarmoederhalskanker en onderstreept het potentieel van antilichaam-geneesmiddelconjugaten (ADC's) in de oncologie.
Werkingsmechanisme van TIVDAK
Tivdak is een ADC dat zich richt op TF door de anti-TF monoklonale antistof tisotumab van Genmab te combineren met de ADC-technologie van Seagen, die is ontworpen om zich te richten op TF-antigenen op kankercellen en de cytotoxische component MMAE rechtstreeks aan kankercellen af te geven.
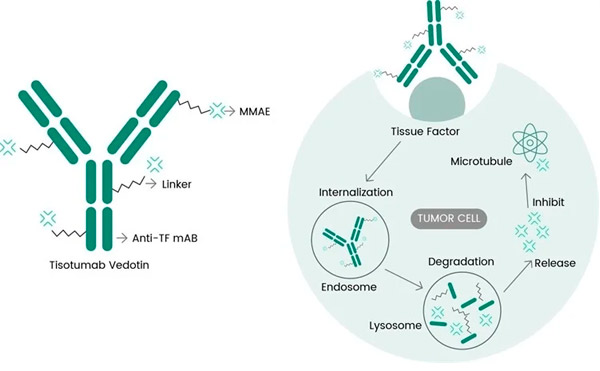
Moleculair werkingsmechanisme van tisotumab vedotin ( https://doi.org/10.3390/ijms23073559 )
TF: Het perfecte doelwit voor ADC-ontwikkeling
Het is bekend dat TF betrokken is bij tumorsignalering en angiogenese en overexpressie vertoont bij de overgrote meerderheid van de patiënten met baarmoederhalskanker en vele andere solide tumoren. Het vermogen om snel te worden opgenomen na antilichaambinding en de minimale impact op de normale bloedstolling vergroten de geschiktheid voor gerichte kankertherapie.
