
Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Hoe een embryo zich in moederlijk weefsel 'bijt': de mechanica van implantatie bij mensen voor het eerst in realtime gefilmd
Laatst beoordeeld: 23.08.2025
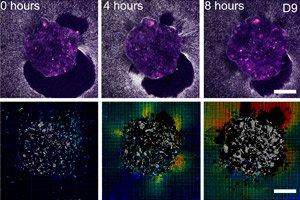 ">
">Wetenschappers uit Barcelona (IBEC, Dexeus Mujer) en Tel Aviv hebben voor het eerst in realtime en in 3D laten zien hoe een menselijk embryo zich hecht aan de "uteriene steiger" en letterlijk het omliggende weefsel trekt en herstructureert. Om dit te doen, creëerden ze een vervormbaar ex vivo platform (collageen/ECM-gels) en pasten ze tractiekrachtmicroscopie rechtstreeks toe op levende menselijke en muizenembryo's. De belangrijkste bevinding: het krachtenpatroon is soortspecifiek en de embryo's zelf zijn mechanosensitief: ze reageren op externe mechanische signalen door het cytoskelet te herstructureren en de groeirichting te veranderen.
Achtergrond van de studie
Implantatie is de 'bottleneck' van de menselijke voortplanting: in dit stadium mislukken zowel natuurlijke concepties als IVF-pogingen het vaakst. Tegelijkertijd is implantatie bij de mens interstitieel: het embryo 'plakt' niet zomaar, maar nestelt zich volledig in het baarmoederslijmvlies – een biochemisch en mechanisch complex proces, dat tot voor kort vrijwel niet werd waargenomen in levende systemen bij de mens. Daarom bleef het mechanisme van hechting en invasie een 'black box', en werden conclusies vaak getrokken op basis van indirecte markers of gegevens uit diermodellen.
De klassieke implantatiebiologie is sterk gebaseerd op de muis, maar er zijn fundamentele verschillen tussen soorten, van de oriëntatie van de blastocyst tot de diepte van de implantatie en het patroon van cellulaire krachten. Bij muizen is de implantatie meer "oppervlakkig", met voorkeursrichtingen voor weefselverplaatsing; bij mensen is het duidelijk invasief, met multifocale trekkrachten rond het embryo. Deze verschillen suggereren dat het muismodel niet altijd schaalbaar is voor mensen, vooral wat betreft de mechanica. Directe observaties van het menselijke embryo in een vervormbare omgeving waren nodig.
De technologische doorbraak werd mogelijk gemaakt door de combinatie van vervormbare 2D/3D-matrices (collageen/ECM) en tractiekrachtmicroscopie met langdurige hoogfrequente beeldvorming. Deze "kunstmatige baarmoeder" maakte het mogelijk om letterlijk te zien en te meten hoe het embryo het omringende weefsel trekt, herstructureert en "uitboort" – en hoe het reageert op externe mechanische signalen (mechanosensitiviteit). Dit opent de weg naar nieuwe criteria voor het beoordelen van het implantatiepotentieel en het verfijnen van de omstandigheden voor embryotransfer.
De context wordt toegepast: als de mechanische eigenschappen van de omgeving en het patroon van embryonale krachten samenhangen met het succes van implantatie, dan is het bij IVF mogelijk om de rigiditeit/samenstelling van de matrix doelbewust te selecteren, rekening te houden met de tijdsintervallen van de transfer en zelfs "kracht"-metrieken te gebruiken als extra selectiemarker. Tegelijkertijd zullen dergelijke platforms helpen bij het verklaren van het percentage vroege zwangerschapsverliezen, wanneer de biochemie "normaal" is, maar de mechanica van hechting niet. Dit alles maakt directe 3D-observaties van menselijke implantatie niet alleen een mooie video, maar ook een nieuw hulpmiddel voor reproductieve geneeskunde.
Waarom is dit belangrijk?
Implantatiefalen is een van de belangrijkste oorzaken van onvruchtbaarheid en tot 60% van de spontane miskramen. Ondanks biochemische vooruitgang in IVF, bleef de mechanica van dit proces bij mensen een "black box". Een nieuwe aanpak stelt ons in staat de krachten en trajecten van embryo-implantatie te zien en biedt een basis voor het verbeteren van embryoselectie en -transferomstandigheden.
Hoe het gedaan werd
De onderzoekers stelden een "kunstmatige baarmoeder" samen - een zachte, transparante en vervormbare omgeving waarin een weefselachtige matrix zichtbaar verschuift onder invloed van embryonale krachten. Vervolgens werden de vezelverplaatsingen met behulp van continue microscopie en computeranalyse geanalyseerd.
- 2D- en 3D-platforms: bij 3D wordt het embryo onmiddellijk in de matrix ingebed (de hechtingsfase wordt ‘overgeslagen’), waardoor het boren in de dikte van het weefsel zichtbaar is.
- Hoge mate van "overleving en penetratie" in 3D: ongeveer 80% succesvolle invasie (beperkt door de nabijheid van glas).
- Tractiekaarten en digitale volumecorrelatie tonen de amplitudes en richtingen van verplaatsingen rond het embryo - in feite een 'afdruk' van de kracht in de loop van de tijd.
Wat is er precies gevonden (kort en puntsgewijs)
1) Soortspecifieke mechanica van implantatie
- Mens: het embryo wordt in de matrix geplaatst, waardoor er meerdere tractiepunten ontstaan en er radiaal gelijkmatige verplaatsingen om zichzelf heen plaatsvinden; de invasiediepte bedraagt maximaal 200 µm.
- Muis: het embryo verspreidt zich voornamelijk over het oppervlak met duidelijke hoofdverplaatsingsrichtingen.
2) Het embryo voelt de mechanismen van de omgeving aan
- Externe krachten → antwoord: bij het menselijk embryo - rekrutering van myosine en gerichte celpseudopodia; bij de muis - rotatie van de implantatie-/groei-as naar de bron van de externe kracht (oriëntatie van de PD-as).
- Mechanosensitieve markers: bij muizen, verschuivingen in YAP-lokalisatie in trofoblast; dit alles wijst op een mechanosensitief feedbackcircuit.
3) De relatie tussen sterkte en succes van implantatie
- Minder verplaatsing van collageen → slechtere implantatievoortgang in menselijke embryo's.
- Integrinen - de "koppelaar" van sterkte: RGD-peptideblokkade/Src-remming bij muizen vermindert de implantatiediepte/-oppervlakte.
Hoe ziet de implementatie eruit?
- Op 2D- en 3D-platforms vormt zich een groeiende ‘halo’ van vezelverplaatsingen rond het embryo; de tractiekaart pulseert alsof het embryo zijn omgeving ‘scant’.
- Op glas vormt het menselijk embryo een platte uitgroei, maar in een zachte matrix blijft het bolvormiger en groeit het dieper - zoals in levend weefsel.
Wat levert dit op voor de praktijk (perspectieven voor IVF en niet alleen)
Het idee is simpel: implantatie is niet alleen "receptorchemie", maar ook de mechanica van adhesie en tractie. Dit betekent dat we het volgende kunnen optimaliseren:
- Materialen en gemiddelde hardheid tijdens kweek-/implantatiepotentiaaltesten;
- Nieuwe markers voor embryoselectie - gebaseerd op trajecten en amplitude van verplaatsingen in de 'slimme' matrix;
- Uterustraining/modulatie (bijvoorbeeld door middel van zachte mechanische signalen) om de hechting te verbeteren zonder agressieve interventies.
Let op: ex vivo werk vindt niet "in de baarmoeder" plaats. Maar juist het feit dat een extern mechanisch signaal de oriëntatie van de implantatie/organisatie van de assen verandert, opent de weg naar gepersonaliseerde embryotransferomstandigheden.
Beperkingen
- Het ex vivo model houdt geen rekening met de immuun-, hormonale en vasculaire dynamiek van het echte endometrium;
- Matrigel/collageen definiëren een reeks eigenschappen (stijfheid, visco-elasticiteit, samenstelling), het is moeilijk om deze met één parameter te veranderen;
- Ethische beperkingen voor studies met mensen (tot 14 dagen) beperken de mogelijkheid tot langetermijnobservatie. De hoge mate van overeenstemming met bekende in-vivo-implantatiemethoden (interstitieel bij mensen versus oppervlakkig bij muizen) vergroot echter het vertrouwen in het model.
Conclusie
Het menselijk embryo "trekt" en "boort" zich actief een weg in het moederlijk weefsel, en mechanische signalen uit de omgeving kunnen zijn gedrag veranderen. Het krachtenpatroon en de implantatiestrategie zijn verschillend bij mensen en muizen – en dit zou kunnen verklaren waarom het muismodel niet altijd een succesvolle implantatie bij mensen voorspelt. Mechanica speelt nu een volwaardige rol in de vroege embryologie en reproductiegeneeskunde.
Bron: Godeau AL et al. Trekkracht en mechanosensitiviteit bemiddelen soortspecifieke implantatiepatronen in menselijke en muizenembryo's. Science Advances 11(33): eadr5199 (15 augustus 2025). DOI: 10.1126/sciadv.adr519
