
Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Studie onthult eiwitinteracties als potentieel pad om ALS te genezen
Laatst beoordeeld: 02.07.2025

In Canada heeft een team onderzoekers van de University of Western Ontario, onder leiding van Dr. Michael Strong, dankzij filantropie een mogelijke remedie voor amyotrofische laterale sclerose (ALS) ontdekt.
Het onderzoek, dat illustreert hoe eiwitinteracties de zenuwceldood die kenmerkend is voor ALS, kunnen beschermen of voorkomen, is het hoogtepunt van tientallen jaren onderzoek dat werd ondersteund door de Temerty Foundation.
"Als arts vind ik het heel belangrijk om tegen een patiënt of familie te kunnen zeggen: 'We proberen deze ziekte te stoppen'", aldus Strong, een klinisch wetenschapper die zijn carrière heeft gewijd aan het vinden van een remedie voor ALS. "Het heeft 30 jaar werk gekost om hier te komen; 30 jaar zorg voor families, patiënten en hun naasten, terwijl we alleen maar hoop hadden. Dat geeft ons reden om te geloven dat we een remedie hebben gevonden."
ALS, ook wel de ziekte van Lou Gehrig genoemd, is een slopende neurodegeneratieve aandoening die de zenuwcellen die verantwoordelijk zijn voor spieraansturing geleidelijk aantast, wat leidt tot spierverlies, verlamming en uiteindelijk de dood. De gemiddelde levensverwachting van een ALS-patiënt na de diagnose is slechts twee tot vijf jaar.
In een studie gepubliceerd in het tijdschrift Brain ontdekte het team van Strong dat het aanpakken van de interactie tussen twee eiwitten in zenuwcellen die door ALS zijn aangetast, de progressie van de ziekte kan stoppen of omkeren. Het team identificeerde ook het mechanisme dat dit mogelijk maakt.
"Belangrijk is dat deze interactie cruciaal kan zijn voor de ontwikkeling van behandelingen, niet alleen voor ALS, maar ook voor andere verwante neurologische aandoeningen, zoals frontotemporale dementie", aldus Strong, die de Arthur J. Hudson hoogleraarschap in ALS-onderzoek bekleedt aan de Schulich School of Medicine and Dentistry van Western University. "Dit is een gamechanger."
Bij bijna alle ALS-patiënten is een eiwit genaamd TDP-43 verantwoordelijk voor de vorming van abnormale klonters in cellen, waardoor deze afsterven. In de afgelopen jaren heeft het team van Strong een tweede eiwit ontdekt, RGNEF, dat TDP-43 tegenwerkt.
De nieuwste doorbraak van het team identificeerde een specifiek fragment van dit RGNEF-eiwit, genaamd NF242, dat de toxische effecten van het ALS-veroorzakende eiwit kan verzachten. De onderzoekers ontdekten dat wanneer de twee eiwitten met elkaar interacteren, de toxiciteit van het ALS-veroorzakende eiwit wordt geëlimineerd, waardoor de schade aan zenuwcellen aanzienlijk wordt verminderd en hun afsterven wordt voorkomen.
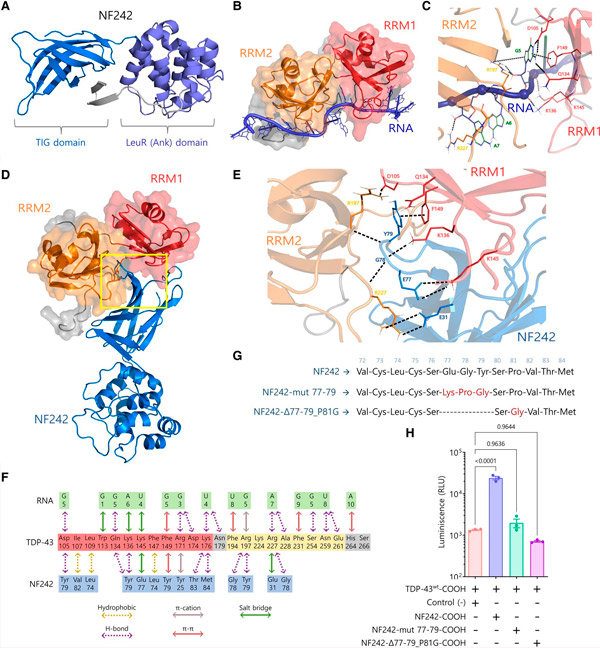
Modellering van de interactie tussen TDP-43 en NF242. Bron: Brain (2024). DOI: 10.1093/brain/awae078
In experimenten met fruitvliegjes leidde deze aanpak tot een significante verlenging van de levensduur, een verbeterde motoriek en bescherming van zenuwcellen tegen degeneratie. Ook in muismodellen leidde de aanpak tot een langere levensduur en mobiliteit, en tot een afname van neuro-inflammatiemarkers.
Het pad naar de ontdekking van het team werd geplaveid door de langetermijninvestering van de familie Temerty in ALS-onderzoek aan de Western University. Strong noemt deze steun 'werkelijk transformerend'.
Nu hebben Strong en zijn team zich ten doel gesteld om hun potentiële behandeling binnen vijf jaar in klinische proeven op mensen te brengen, dankzij een nieuwe donatie van de Temerty Foundation.
Het fonds, opgericht door James Temerty, oprichter van Northland Power Inc., en Louise Arcand Temerty, investeert $ 10 miljoen over een periode van vijf jaar om de volgende stappen te ondersteunen om deze behandeling beschikbaar te maken voor ALS-patiënten.

Dr. Michael Strong, die de Arthur J. Hudson-leerstoel voor ALS-onderzoek bekleedt aan de Schulich School of Medicine and Dentistry van de Western University, heeft een eiwit ontdekt dat zou kunnen leiden tot een remedie voor ALS. Foto: Allan Lewis / Schulich School of Medicine and Dentistry
"Het vinden van een effectieve behandeling voor ALS zou enorm veel betekenen voor mensen die met deze vreselijke ziekte leven en hun naasten", aldus James Temerty. "Western University verlegt de grenzen van de kennis over ALS en we zijn verheugd om bij te dragen aan de volgende fase van dit baanbrekende onderzoek."
Dankzij de nieuwe donatie van de Temerty Foundation bedraagt de totale investering van de familie in onderzoek naar neurodegeneratieve ziekten aan de Western University $ 18 miljoen.
"Dr. Strongs onvermoeibare toewijding aan zijn zaak wordt geëvenaard door de diepe wens van de familie Temerty om een verschil te maken voor de duizenden mensen wereldwijd bij wie deze verwoestende ziekte is vastgesteld", aldus Alan Shepard, president van Western University. "De investering en visie van de Temerty Foundation hebben de vooruitgang in het vinden van een effectieve behandeling voor ALS versneld. We zijn de familie Temerty dankbaar voor hun inzet voor levensveranderend onderzoek."
"Dit is een keerpunt in ALS-onderzoek dat de potentie heeft om het leven van patiënten werkelijk te veranderen", aldus dr. John Yu, decaan van de Schulich School of Medicine and Dentistry.
Dankzij het leiderschap van Dr. Strong, onze voortdurende investering in de beste instrumenten en technologie, en de steun van de Temerty Foundation, zijn we verheugd een nieuw tijdperk van hoop voor ALS-patiënten aan te kondigen.
De resultaten van het werk worden gedetailleerd beschreven in een artikel gepubliceerd in het tijdschrift Brain.
