
Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Hepatitis A-virus
Medisch expert van het artikel
Laatst beoordeeld: 04.07.2025
Virale hepatitis A is een infectieziekte bij mensen, die voornamelijk wordt gekenmerkt door leverschade en zich klinisch manifesteert door intoxicatie en geelzucht. Het hepatitis A-virus werd in 1973 ontdekt door S. Feinstone (et al.) met behulp van immuun-elektronenmicroscopie en door apen - chimpansees en zijdeaapjes - te infecteren. De essentie van de immuun-elektronenmicroscopie is dat specifieke antilichamen (convalescent serum) worden toegevoegd aan het filtraat van de ontlasting van een patiënt met hepatitis A en dat het sediment aan elektronenmicroscopie wordt onderworpen. Door de interactie van virussen met specifieke antilichamen ondergaan ze een specifieke aggregatie. In dit geval zijn ze gemakkelijker te detecteren, en aggregatie onder invloed van antilichamen bevestigt de specificiteit van de ziekteverwekker. De ontdekking van S. Feinstone werd bevestigd in experimenten met vrijwilligers.
Het hepatitis A-virus is bolvormig, de viriondiameter is 27 nm. Het genoom wordt weergegeven door enkelstrengs positief RNA met mm 2,6 MD. Er is geen supercapside. Het symmetrietype is kubisch - icosaëder. De capside heeft 32 capsomeren en wordt gevormd door vier polypeptiden (VP1-VP4). Volgens zijn eigenschappen behoort het hepatitis A-virus tot het geslacht Heparnovirus, de familie Picornaviridae. Qua antigenen is het hepatitis A-virus (HAV - hepatitis A-virus) homogeen. HAV reproduceert goed in het lichaam van chimpansees, bavianen, mantelbavianen en zijdeaapjes. Lange tijd kon het virus niet worden gekweekt. Pas in de jaren 1980 was het mogelijk om celculturen te verkrijgen waarin HAV reproduceert. Aanvankelijk werden hiervoor continue cellijnen van embryonale nieren van resusaapjes (cultuur FRhK-4) gebruikt, en nu wordt er een continue cellijn van niercellen van groene meerkatten (cultuur 4647) gebruikt.
Op basis van de aanbevelingen van WHO-experts is de volgende nomenclatuur van hepatitis A-virusmarkers aangenomen: hepatitis A-virus - HAV-antilichamen tegen hepatitis A-virus: anti-HAV IgM en anti-HAV IgG.
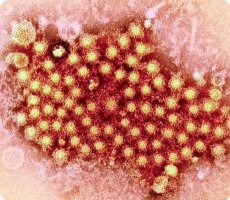
HAV is een klein deeltje met een diameter van 27-30 nm, icosahedraal symmetrisch en homogeen. Het elektronogram, verkregen met de immuunaggregatiemethode, toont elektronendichte deeltjes met oppervlakkig gelegen, symmetrisch gerangschikte capsomeren. Bij negatief contrast worden zowel volle als lege deeltjes in de preparaten zichtbaar. Het nucleocapside van HAV heeft, in tegenstelling tot dat van influenza, geen uitsteeksels aan het oppervlak en geen membraan. Belangrijk is ook dat het HAV-virion geen hartvormige structuur heeft.
Op basis van zijn fysisch-chemische eigenschappen wordt het hepatitis A-virus geclassificeerd als behorend tot de picornavirusfamilie, het enterovirusgeslacht met serienummer 72. Deze taxonomie bleek echter te ongebruikelijk en de WHO achtte het mogelijk om de terminologie "hepatitis A-virus" te behouden.
Zoals alle virussen van de familie Picornaviridae bevat het hepatitis A-virus ribonucleïnezuur. Sommige laboratoria hebben de mogelijkheid aangetoond om het hepatitis A-virusgenoom te klonen, wat de mogelijkheid opent om vaccins te verkrijgen.
Resistentie tegen het hepatitis A-virus
Het virus is relatief resistent tegen hoge temperaturen, zuren, vetoplosmiddelen (geen lipiden) en desinfectiemiddelen, en verdraagt lage temperaturen goed. Dit alles draagt bij aan de langdurige bewaring ervan in de buitenlucht. Bij kamertemperatuur overleeft het enkele weken, bij 60 °C verliest het gedeeltelijk zijn besmettelijkheid na 4-12 uur en volledig na enkele minuten bij 85 °C. Het is zeer resistent tegen chloor, waardoor het via de barrières van waterzuiveringsinstallaties in het leidingwater kan doordringen.
Als we alle gegevens samenvatten, kunnen we het hepatitis A-virus als volgt karakteriseren:
- de natuurlijke gastheer is de mens;
- proefdieren - zijdeaapjes, chimpansees;
- de bron van de infectie is ontlasting;
- de ziekte is epidemisch en endemisch;
- transmissieroute: feco-oraal;
- incubatieperiode - 14-40 dagen;
- overgang naar chronische hepatitis - niet waargenomen.
De immunologische eigenschappen van HAV zijn als volgt:
- Prototypische stammen - Ms-1, CR-326, GВG. Allen zijn immunologisch vergelijkbaar of identiek;
- Antilichamen - IgM en IgG - worden geproduceerd als reactie op de introductie van structurele eiwitten van het virus en hebben een beschermende werking;
- I. Het beschermende effect van menselijk serum gammaglobuline: het voorkomt of verzwakt de ziekte als het wordt toegediend vóór de infectie of tijdens de incubatieperiode.
De fysisch-chemische eigenschappen van NAU zijn als volgt:
- Morfologie: schelploos bolvormig deeltje met kubische symmetrie, capside bestaat uit 32 capsomeren;
- Diameter - 27-30 nm;
- Dichtheid in CsCl (g/cm3) - 1,38-1,46 (open deeltjes), 1,33-1,34 (volwassen virion), 1,29-1,31 (onvolwassen virionen, lege deeltjes);
- Sedimentatiecoëfficiënt - 156-160 volwassen virionen;
- Nucleïnezuur is een enkelstrengs, lineair RNA;
- Relatief moleculair gewicht - 2,25 106-2,8 106KD;
- Het aantal nucleotiden bedraagt 6.500-8.100.
De stabiliteit van HAV onder fysische en chemische invloeden is als volgt:
- Chloroform, ether - stabiel;
- Chloor, 0,5-1,5 mg/l, 5 °C, 15 min - gedeeltelijke inactivering;
- Chloramine, 1 g/l, 20 °C, 15 min - volledige inactivering;
- Formaline, 1:4000, 35-37 °C, 72 h - volledige inactivatie, 1:350, 20 °C, 60 min - gedeeltelijke inactivatie.
Temperatuur:
- 20-70 °C - stabiel;
- 56 °C, 30 min - stabiel;
- 60 °C, 12 uur - gedeeltelijke inactivering;
- 85 °C, 1 min - volledige inactivering;
- Autoclaveren, 120 °C. 20 min - volledige inactivering;
- Droge hitte, 180 °C, 1 uur - volledige inactivering;
- UFO, 1,1 W, 1 min - volledige inactivering.
De gepresenteerde gegevens tonen aan dat het hepatitis A-virus qua fysicochemische eigenschappen het dichtst bij enterovirussen staat. Net als andere enterovirussen is HAV resistent tegen veel desinfectiemiddelen en wordt het binnen enkele minuten volledig geïnactiveerd bij 85 °C en autoclavering.
Het is bewezen dat het hepatitis A-virus zich kan voortplanten in primaire en continue monolaaglijnen van menselijke en apencelculturen. Een bijzonder actieve voortplanting van het hepatitis A-virus in in-vitroculturen wordt waargenomen wanneer leverextracten van zieke apen als uitgangsmateriaal worden gebruikt. Opgemerkt dient echter te worden dat bij alle experimenten met de voortplanting van het hepatitis A-virus in in-vitroculturen de aandacht wordt gevestigd op de lange incubatietijd tijdens primaire passages (tot 4-10 weken). Vervolgens neemt de accumulatie van viraal genetisch materiaal toe, maar de absolute waarden blijven zeer onbeduidend. Dit geeft veel onderzoekers aanleiding om te spreken van onvolledige replicatie van het hepatitis A-virus in weefselculturen.
Samenvattend kunnen we stellen dat de literatuurgegevens over de reproductie van het hepatitis A-virus in extra-weefselculturen buiten beschouwing blijven en dat de overleving van HAV in vitro op lange termijn buiten kijf staat. De optimale omstandigheden voor een stabiele, hoge mate van virusreplicatie zijn nog niet definitief vastgesteld, wat de studie van de biologische eigenschappen en het verkrijgen van een bron van reagentia voor de productie van diagnostiek en vaccinontwerp belemmert.
Tegelijkertijd zijn er in de literatuur optimistischere oordelen over dit probleem te vinden. De oplossing van alle problemen met betrekking tot de kweek van het hepatitis A-virus is een kwestie van de nabije toekomst. Bij het bestuderen van de optimale omstandigheden voor de reproductie van HAV in de kweek van embryonale niercellen van de resusaap werden twee fasen geïdentificeerd: de fase van productie van het infectieuze virus (tot 6-8 dagen ter hoogte van de vijfde passage) en de fase van intensieve accumulatie van het virale antigeen. Er werd ook aangetoond dat de meest significante accumulatie van het virale antigeen plaatsvindt onder de omstandigheden van de zogenaamde rolkweek (roterende kolven). Deze methode opent ruime mogelijkheden voor het verkrijgen van kweekantigeen in grote hoeveelheden, en daarmee zal het bronmateriaal voor de bereiding van diagnostische systemen en de productie van vaccins ontstaan.
Epidemiologie van hepatitis A
Het hepatitis A-virus is zeer pathogeen voor mensen. Volgens de WHO (1987) is een infectie met slechts één virion voldoende om de ziekte te veroorzaken. De praktische infectieuze dosis is echter waarschijnlijk veel hoger. De enige bron van infectie is een geïnfecteerd persoon. Het virus wordt in grote hoeveelheden uitgescheiden met de ontlasting 12-14 dagen vóór het begin van geelzucht en gedurende de 3 weken van de icterische periode. Er zijn geen significante verschillen gevonden in de uitscheiding van de ziekteverwekker bij patiënten met icterische, anicterische en asymptomatische vormen van hepatitis A. De infectieweg is fecaal-oraal, voornamelijk via water, evenals via huishouden en voedsel. De belangrijkste (primaire) transmissieroute van het virus is via water. Infectie via druppeltjes in de lucht is ook mogelijk. De vatbaarheid van de bevolking is universeel. Meestal worden kinderen jonger dan 14 jaar getroffen. De ziekte heeft een uitgesproken herfst-winterseizoenskarakter.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Symptomen van hepatitis A
De incubatietijd varieert van 15 tot 50 dagen, afhankelijk van de infectieuze dosis van het virus, maar bedraagt gemiddeld 28-30 dagen. Eenmaal in het lichaam vermenigvuldigt het hepatitis A-virus zich in de regionale lymfeklieren, dringt het door in het bloed en vervolgens in de levercellen en veroorzaakt acute diffuse hepatitis, die gepaard gaat met schade aan hepatocyten en reticulo-endotheliale elementen van de lever en een afname van de ontgiftings- en barrièrefunctie. Schade aan hepatocyten ontstaat niet door de directe werking van het virus, maar als gevolg van immunopathologische mechanismen. Het meest typische beeld van hepatitis A is een acute icterische cyclische vorm: incubatieperiode, prodromale (pre-icterische), icterische periode en herstel. In de infectiehaarden wordt echter een groot aantal patiënten met anicterische en asymptomatische vormen van infectie aangetroffen, waarvan het aantal aanzienlijk groter is dan icterische vormen ("ijsbergfenomeen").
De immuniteit na infectie is sterk en langdurig en wordt veroorzaakt door virusneutraliserende antilichamen en immuungeheugencellen.
Microbiologische diagnostiek van hepatitis A
Diagnostiek van hepatitis A (met uitzondering van infecties bij dieren - chimpansees, zijdeaapjes, bavianen, die we niet hebben) is gebaseerd op verschillende immunologische methoden: RSC, immunofluorescentiemethode, hemagglutinatie van immuunadhesie (het complex van viraal antigeen + antilichaam in aanwezigheid van complement wordt geadsorbeerd aan erytrocyten en veroorzaakt hun verkleving). De gebruiksmogelijkheden van deze methoden zijn echter beperkt vanwege het gebrek aan specifieke virale antigenen, en de immunofluorescentiereactie vereist een leverbiopsie, wat ongewenst is. De immuunelektronenmicroscopie is betrouwbaar en specifiek, maar zeer arbeidsintensief. Daarom is de enige acceptabele immunologische reactie tot nu toe de immunosorbensanalyse van de vaste fase in de vorm van IFM of RIM, met name bij de modificatie van "capture" van immunoglobulinen van klasse M. In ons land is hiervoor een testsysteem voorgesteld: "DIAGN-A-HEP". Het werkingsprincipe van dit testsysteem is als volgt. Eerst worden antilichamen tegen immunoglobulinen van klasse M (anti-immunoglobulinen M) gesorbeerd aan de wanden van polystyreenputjes, waarna het te testen serum van de patiënt wordt toegevoegd. Als het IgM-antilichamen bevat, zullen deze zich binden aan anti-antilichamen van klasse M. Vervolgens wordt een specifiek viraal antigeen (hepatitis A-virus) toegevoegd, dat wordt verkregen door kweek in celkweek. Het systeem wordt gewassen en er worden antivirale antilichamen, gelabeld met mierikswortelperoxidase, aan toegevoegd. Als alle vier componenten van het systeem interacteren, ontstaat er een vierlaagse "sandwich":
- antiimmunoglobulinen M,
- immunoglobulinen M (tegen het hepatitis A-virus - in het serum van de onderzochte patiënt),
- viraal antigeen,
- enzym-gelabelde antivirale antilichamen.
Om dit complex te detecteren, wordt een substraat voor het enzym aan de wells toegevoegd. Onder invloed van het enzym wordt het afgebroken en ontstaat een gekleurd product. De kleurintensiteit kan kwantitatief worden gemeten met een spectrofotometer of fotocolorimeter.
Het voordeel van de IgM-"capture"-methode is dat antilichamen van deze klasse immunoglobulinen verschijnen tijdens de primaire immuunrespons en het actieve stadium van de infectie aangeven; ze verdwijnen nadat de ziekte is doorgemaakt. Antivirale antilichamen die tot de IgG-klasse behoren, blijven daarentegen lang na het doormaken van de ziekte aanwezig en zorgen voor verworven immuniteit. Er is een DNA-probemethode voorgesteld voor de detectie van het hepatitis A-virus: complementair vRNA-DNA wordt als probe gebruikt.
Specifieke preventie van hepatitis A
De voorheen veelgebruikte seroprofylaxe van hepatitis A met gammaglobuline was niet gerechtvaardigd, daarom werd de nadruk gelegd op het uitvoeren van vaccinatieprofylaxe. Vaccinatie tegen hepatitis A vindt plaats. Hiervoor zijn verschillende soorten vaccins in ontwikkeling en worden al gebruikt. In Rusland werd in 1995 een effectief vaccin tegen hepatitis A verkregen, dat nu met succes wordt gebruikt.

