
Alle iLive-inhoud wordt medisch beoordeeld of gecontroleerd op feiten om zo veel mogelijk feitelijke nauwkeurigheid te waarborgen.
We hebben strikte richtlijnen voor sourcing en koppelen alleen aan gerenommeerde mediasites, academische onderzoeksinstellingen en, waar mogelijk, medisch getoetste onderzoeken. Merk op dat de nummers tussen haakjes ([1], [2], etc.) klikbare links naar deze studies zijn.
Als u van mening bent dat onze inhoud onjuist, verouderd of anderszins twijfelachtig is, selecteert u deze en drukt u op Ctrl + Enter.
Herpetische encefalitis
Medisch expert van het artikel
Laatst beoordeeld: 04.07.2025
De kans op een infectie met het herpes simplexvirus is zeer groot. Aangenomen wordt dat de overgrote meerderheid van de volwassen wereldbevolking seropositief is voor labiale herpes. De verraderlijkheid van deze intracellulaire parasiet is dat hij lang latent aanwezig kan blijven en, onder gunstige omstandigheden voor zijn ontwikkeling, het centrale zenuwstelsel kan aantasten.
Encefalitis is een ontsteking van het hersenparenchym met neurologische disfunctie die kan worden veroorzaakt door infectieuze, postinfectieuze en niet-infectieuze oorzaken.[ 1 ] Infectie is verantwoordelijk voor ongeveer 50% van de identificeerbare gevallen en is de meest voorkomende etiologische categorie van encefalitis.[ 2 ]
Herpetische encefalitis is een vrij zeldzame en ernstige ziekte, waarvan de meeste gevallen worden veroorzaakt door het virus van het eerste type. Bij gebrek aan tijdige diagnose en antivirale therapie gaat de ziekte gepaard met een hoge mortaliteit en een groot aantal ernstige neurologische complicaties die gepaard gaan met lokale aantasting van het limbisch systeem van de hersenen.
Het woord herpes vertaalt zich als "kruipend" of "kruipend" en verwijst naar herpetische huidletsels. Goodpasture [ 3 ] en anderen toonden aan dat materiaal van herpetische labiale en genitale letsels encefalitis veroorzaakte wanneer het werd geïnoculeerd in het littekenweefsel van het hoornvlies of de huid van konijnen. In de jaren 1920 was de Mathewson Commission een van de eersten die rapporteerde dat HSV encefalitis bij mensen veroorzaakte. Het eerste pediatrische rapport over HSVE werd gepubliceerd in 1941. [ 4 ] Het eerste volwassen geval, een 25-jarige man met hoofdpijn, koorts, afasie en verwijde linkerpupil, werd gerapporteerd in 1944. [ 5 ] Postmortale pathologie onthulde talrijke petechiën en ecchymosen met perivasculaire lymfocytaire manchetten in de linker temporaalkwab, middenhersenen en lumbale wervelkolom. Intranucleaire insluitsels werden geïdentificeerd en het virus werd geïsoleerd uit de hersenen van de patiënt. Sinds deze eerste rapporten is er aanzienlijke vooruitgang geboekt in de pathofysiologie, diagnose en behandeling van HSVE.
Epidemiologie
Herpetische encefalitis treft wereldwijd jaarlijks twee tot vier op de miljoen mensen. Van alle gevallen van encefalitis met verschillende oorzaken vertegenwoordigt herpetische encefalitis ongeveer 15%; dit percentage fluctueert van jaar tot jaar lichtjes.
In 60-90% van de gevallen wordt bij patiënten het herpesvirus HSV-1 aangetroffen. [ 6 ] De meeste deskundigen zien geen verband tussen de incidentie van de ziekte en het seizoen van het jaar, maar sommigen hebben aangegeven dat herpes encefalitis vaker in de lente voorkomt.
Iedereen, ongeacht geslacht en leeftijd, kan ziek worden. Ongeveer een derde van de gevallen doet zich echter voor in de kindertijd en adolescentie (tot 20 jaar), en de helft betreft patiënten die de leeftijd van een halve eeuw al gepasseerd zijn.
Hoewel encefalitis zeldzaam is bij geïnfecteerde individuen, is HSV-1 wereldwijd consequent de meest voorkomende oorzaak van sporadische encefalitis.[ 7 ],[ 8 ] De incidentie van HSV wereldwijd wordt geschat op 2 tot 4 gevallen per 1.000.000,[ 9 ] en de incidentie in de Verenigde Staten is vergelijkbaar. Er is een bimodale verdeling met een piekincidentie bij kinderen (<3 jaar) en opnieuw bij volwassenen >50 jaar, maar de meeste gevallen komen voor bij individuen ouder dan 50 jaar, ongeacht het geslacht.[ 10 ],[ 11 ]
Oorzaken herpetische encefalitis
De meeste deskundigen zijn geneigd te geloven dat de ontwikkeling van deze ziekte het gevolg is van de activering van herpesvirussen, die latent aanwezig zijn en zich hebben geïntegreerd in de DNA-ketens van zenuwweefselcellen.
Een primaire infectie met HSV-1 of HSV-2 kan optreden in de vorm van een ontstekingsproces in de cortex, subcortex en witte stof van de hersenen en de enige manifestatie van de infectie zijn. Dergelijke gevallen zijn typisch voor de eerste confrontatie met het herpesvirus in de kindertijd en adolescentie.
Een diffuse infectie met het herpes simplexvirus kan, wanneer de viscerale organen en de huid bij het proces betrokken zijn, zich vaak uitbreiden naar het centrale zenuwstelsel, wat kan leiden tot de ontwikkeling van encefalitis.
Bij de overgrote meerderheid van de patiënten met herpetische ontsteking van de hersensubstantie wordt het herpes simplexvirus type 1 (HSV-1) aangetroffen, dat zich manifesteert als jeukende blaasjes op de lippen, veel minder vaak het tweede (HSV-2), het zogenaamde genitale virus. Bij chronische, trage encefalitis worden HSV-3 (herpes zoster, dat waterpokken/gordelroos veroorzaakt), HSV-4 (het Epstein-Barr-virus, dat de ziekte van Filatov of mononucleosis infectiosa veroorzaakt), cytomegalovirus HSV-5 en de humane herpesvirussen HSV-6 en HSV-7 aangetroffen, die "opvallen" bij de ontwikkeling van het chronisch vermoeidheidssyndroom. Soms worden bij één patiënt cellen van verschillende weefsels aangetast door virussen van verschillende stammen (mengvorm). Theoretisch gezien kan schade door al deze typen dus leiden tot herpetische encefalitis.
Een complicatie in de vorm van een hersenontsteking wordt soms veroorzaakt door de zogenaamde herpetische angina pectoris. Strikt genomen heeft deze ziekte niets te maken met het herpesvirus. De encefalitis die tegen deze achtergrond optreedt, is dus viraal, maar niet herpetisch. De verwekker is het Coxsackievirus - een enterovirus. Wat het verwant maakt aan herpes is hun virale aard - het vermogen om te parasiteren in cellen, waaronder de hersenen. Hetzelfde geldt voor een ziekte als herpetische stomatitis. In feite is de zogenaamde herpetische angina pectoris (stomatitis) dezelfde ziekte, alleen is bij angina pectoris het slijmvlies van de keelholte sterker aangetast; er verschijnen blaasjes op die lijken op herpes. Bij stomatitis is het slijmvlies van de mondholte sterker aangetast. De moderne geneeskunde noemt deze pathologie enterovirus vesiculaire faryngitis of stomatitis, afhankelijk van de overheersende plek van de uitslag en de daarmee gepaard gaande pijn. Deze ziekten genezen over het algemeen goed en genezen volledig. In zeldzame gevallen kunnen er echter complicaties optreden in de vorm van virale encefalitis, waarvan de symptomen identiek zijn aan die van herpes.
Herpesvirussen die menselijke huidcellen of slijmvliezen van de orolabiale zone aantasten, nestelen zich in deze cellen, beginnen zich te vermenigvuldigen en migreren door het lichaam via hematogene en lymfogene routes, waarbij ze zenuwcellen bereiken. Na onderdrukking van de actieve fase die zich na infectie ontwikkelt, nestelen de virussen zich in hun genetisch apparaat en blijven ze in een "slapende" toestand in de zenuwcellen, vermenigvuldigen zich niet en manifesteren zich niet bij de meeste dragers. In studies met postmortale oligonucleotide-onderzoek werd DNA van het herpes simplex-virus aangetroffen in neuronen van het hersenweefsel van de meeste overledenen, van wie de doodsoorzaak absoluut niet verband hield met een infectie met dit micro-organisme. Het is vastgesteld dat de introductie van het herpesvirus in cellen, met name zenuwweefsel, niet altijd gepaard gaat met reproductie en de dood van de gastheercel. Meestal remt het de replicatie van de vreemde en gaat het micro-organisme in een incubatietoestand.
Maar onder invloed van bepaalde uitlokkende factoren wordt het herpesvirus geactiveerd en verandert het latente verloop van de infectie in een acuut of subacuut proces, waarbij het hersenweefsel niet noodzakelijkerwijs wordt aangetast.
Risicofactoren
De risicofactoren die het reactivatieproces in gang zetten, zijn niet nauwkeurig vastgesteld. Aangenomen wordt dat dit lokale verwondingen in het gezicht, stress, onderkoeling of oververhitting, immunosuppressie, hormonale schommelingen, frequente vaccinaties en onvoorzichtig gedrag na vaccinaties kunnen zijn. Leeftijd speelt een rol: baby's en ouderen lopen het grootste risico op het ontwikkelen van herpes encefalitis.
Pathogenese
De pathogenese van herpes encefalitis is niet uniform. Aangenomen wordt dat bij mensen die voor het eerst geïnfecteerd zijn (kindertijd en adolescentie), het herpes simplex virus type 1 de cellen van de hersensubstantie binnendringt vanuit het epitheel van het slijmvlies van de neuskeelholte. Nadat het micro-organisme de weefselbarrière heeft gepasseerd, migreert het neurogeen (langs de neuriten van de reukneuronen) naar de bulbus olfactorius en veroorzaakt daar, onder gunstige omstandigheden voor zijn ontwikkeling, een ontsteking van de hersensubstantie.
De mechanismen waarmee HSV toegang krijgt tot het centrale zenuwstelsel (CZS) bij mensen zijn onduidelijk en blijven onderwerp van discussie. De meest waarschijnlijke routes omvatten retrograde transport via de nervus olfactorius of nervus trigeminus [ 12 ], [ 13 ] of via hematogene verspreiding. Viraal tropisme van de orbitofrontale en mesotemporale kwabben spreekt in de meeste gevallen hematogene verspreiding tegen. Experimentele gegevens bij dieren ondersteunen transmissie naar het CZS via één of beide van de trigeminus en olfactorische routes en suggereren dat virionen zich via de voorste commissuur naar de contralaterale temporaalkwab kunnen verspreiden. [ 14 ]
In tegenstelling tot andere hersenzenuwen met sensorische functies, lopen de reukzenuwbanen niet door de thalamus, maar maken ze direct verbinding met de frontale en mesotemporale kwabben (inclusief het limbisch systeem). Er is enig bewijs dat de reukfunctie zich bij mensen uitbreidt naar het CZS, maar definitieve gegevens ontbreken.[ 15 ],[ 16 ] De trigeminuszenuw innerveert de hersenvliezen en kan zich uitstrekken tot in de orbitofrontale en mesiotemporale kwabben.[ 17 ] Aangezien de sensorische kernen van de trigeminus zich echter in de hersenstam bevinden, zou men verwachten dat de relatief zeldzame HSVE-geassocieerde hersenstamencefalitis vaker zou voorkomen als dit in de meeste gevallen de primaire toegangsroute naar het CZS zou zijn.[ 18 ],[ 19 ]
Of HSVE een reactivatie is van latent virus of wordt veroorzaakt door een primaire infectie is ook onderwerp van discussie; beide kunnen voorkomen. Voorgestelde pathogenische mechanismen omvatten reactivatie van latent HSV in de trigeminusganglia met daaropvolgende verspreiding van de infectie naar de temporale en frontale kwabben, primaire CZS-infectie, of mogelijk reactivatie van latent virus in het hersenparenchym zelf.[ 20 ],[ 21 ] In ten minste de helft van de HSVE-gevallen is de virale stam die verantwoordelijk is voor encefalitis anders dan de stam die herpesachtige huidletsels veroorzaakt bij dezelfde patiënt, een observatie die de mogelijkheid van een primaire CZS-infectie suggereert.[ 22 ]
Nederlands Een HSV-infectie veroorzaakt een sterke reactie van het aangeboren immuunsysteem totdat het adaptieve immuunsysteem de actieve infectie kan helpen elimineren. Vroeg in de immuunreactie op HSV herkennen patroonherkenningsreceptoren, Toll-like receptoren (TLR's) genaamd, die zich op cellen van het aangeboren immuunsysteem bevinden, pathogeen-geassocieerde moleculaire patronen en binden zich eraan. [ 23 ] Dit veroorzaakt TLR-dimerisatie, wat vervolgens signaalroutes activeert die de productie van pro-inflammatoire cytokinen zoals interferonen (IFN's), tumornecrosefactor en verschillende interleukinen initiëren. [ 24 ] IFN's dragen bij aan de resistentie van de gastheer tegen virale proliferatie door activering van de Jak-Stat-signaalroute [ 25 ] en door de productie te activeren van zowel RNase-enzymen die cellulair RNA (zowel van de gastheer als viraal) afbreken als dubbelstrengs RNA-afhankelijke proteïnekinase, die de cellulaire translatie stopt. [ 26 ] Tekorten in de immuunrespons op HSV (bijvoorbeeld defecten in het TLR-3-pad, waaronder TLR3 zelf, UNC93B1, TIR-domein-bevattende adaptor-inducerende IFN-β, tumornecrosefactorreceptor-gerelateerde factor-3, TANK-bindende kinase 1, of IFN-regulerende factor-3) maken de gastheer vatbaar voor HSVE. [ 27 ], [ 28 ]
De ontstekingscascade activeert adaptieve immuniteit, wat kan leiden tot necrose en apoptose van geïnfecteerde cellen. Hoewel de immuunrespons van de gastheer cruciaal is voor de uiteindelijke virale controle, kan de ontstekingsreactie, met name de rekrutering van geactiveerde leukocyten, bijdragen aan weefselvernietiging en daaropvolgende neurologische gevolgen.[ 29 ],[ 30 ]
Nederlands Na de primaire infectie stelt het virus een latente toestand in voor de rest van het leven van de gastheer en blijft inactief tenzij het wordt gereactiveerd.[ 31 ] Om latentie te bewerkstelligen en te behouden, moeten een aantal complexe processen in evenwicht worden gebracht. Deze omvatten het uitschakelen van virale genen in de lytische fase, het uitschakelen van de verdedigingsmechanismen van de gastheercel (bijv. apoptose) en het ontwijken van de immuniteit van de gastheer, inclusief zowel aangeboren als adaptieve immuunreacties (bijv. downregulatie van de expressie van het grote histocompatibiliteitscomplex).[ 32 ],[ 33 ] HSV-specifieke CD8+ T-cellen bevinden zich in de trigeminusganglia en dragen bij aan het behoud van virale latentie.[ 34 ] Tijdens reactivatie vindt virale genexpressie plaats op een tijdelijk georganiseerde manier, zoals onlangs is besproken. [ 35 ] Na reactivatie kan het virus aangrenzende neuronen infecteren en zich verplaatsen naar weefsels die worden geïnnerveerd door geïnfecteerde dorsale wortelganglia, wat een terugval van de ziekte veroorzaakt en infectieuze virale deeltjes vrijgeeft die kunnen worden overgedragen op anderen.
In de vroege kindertijd wordt het HSV-2-virus het vaakst vastgesteld. De meeste infecties vinden plaats tijdens de passage van het kind door het geboortekanaal van de moeder, als zij zich in de acute fase van de ziekte bevindt (er is sprake van huiduitslag op de geslachtsdelen). De kans op infectie tijdens de geboorte is het grootst, dus vrouwen met acute genitale herpes wordt meestal geadviseerd om via een keizersnede te bevallen.
Veel zeldzamer is herpes encefalitis bij pasgeborenen het gevolg van een intra-uteriene infectie. Ook contact met een zieke ouder of een medewerker van het kraamkliniek na de geboorte kan de oorzaak zijn. Toch komen zulke gevallen veel minder vaak voor.
Volwassen patiënten met deze neuro-infectie hadden meestal in het verleden herpesuitslag of waren volgens de testresultaten seropositief voor het herpes simplexvirus. Encefalitis kan zich ontwikkelen bij herhaalde infectie met een andere virusstam - in dit geval wordt een andere stam van het herpesvirus aangetroffen op het slijmvlies van de mondholte of keelholte (neus), dan de stam die het hersenweefsel heeft aangetast. Bij ongeveer een kwart van de patiënten met herpes encefalitis worden andere stammen aangetroffen.
Driekwart van de overige patiënten heeft orolabiale stammen van het virus die identiek zijn aan die in het hersenweefsel. In dit geval worden twee scenario's verondersteld. De eerste optie gaat uit van de hypothese dat het virus latent aanwezig is in de knooppunten van de nervus trigeminus of in de sympathische zenuwen, en dat het bij neurogene reactivering (langs de zenuwen die de middelste schedelgroeve innerveren) het hersenweefsel bereikt. De tweede optie gaat ervan uit dat het virus na infectie de neuronen in de hersenen al heeft bereikt en zich daar in een latente toestand bevond, waar het onder gunstige omstandigheden werd gereactiveerd.
De replicatie van het herpesvirus vindt intracellulair plaats, met de vorming van intranucleaire insluitsels, die neuronen en hulpcellen (glia) aantasten en interneuronale verbindingen vernietigen.
Hoe wordt herpes encefalitis overgedragen?
Nauw contact met een patiënt vormt geen gevaar voor directe infectie met herpes encefalitis. Alleen het virus zelf wordt overgedragen. Meestal gebeurt dit tijdens direct contact met een geïnfecteerd persoon in de acute fase, wanneer deze orolabiale, genitale of huiduitslag heeft. Niet voor niets wordt herpes ook wel de "kusziekte" genoemd. Vloeibaar vocht uit de ophoping van blaasjes op de lippen van de patiënt is simpelweg oververzadigd met virussen; zijn speeksel en neusafscheiding zijn eveneens besmet met ziekteverwekkers. De infectie tast een beschadigde huid aan (met microscheurtjes, krassen) wanneer druppeltjes speeksel, besmet met micro-organismen of rhinobronchiale afscheiding, in de huid terechtkomen tijdens hoesten en niezen, tijdens een emotioneel gesprek of tijdens direct contact, bijvoorbeeld bij zoenen. Bij jonge kinderen kan het virus zelfs door een intacte huid heen dringen. Besmetting is mogelijk door afwisselend dezelfde handdoek, vaat, lippenstift en andere soortgelijke handelingen te gebruiken.
Je kunt het eerste en tweede type cellulaire parasiet oplopen tijdens orale-genitale seks met een geïnfecteerde partner. En als de blaasjes op de lippen duidelijk zichtbaar zijn, is het vaak lastig om de actieve fase van HSV-2 (seksueel) te bepalen, aangezien de meeste geïnfecteerde mensen latente exacerbaties kunnen hebben en de patiënt zelf het misschien niet vermoedt.
Het is ook mogelijk om in het latente stadium besmet te raken. Dit gebeurt meestal door frequent direct contact met slijmvliezen of door verwondingen en microbeschadigingen aan de contactoppervlakken van het lichaam van een gezond persoon.
Genitale herpes wordt overgedragen van een moeder die tijdens de zwangerschap besmet raakt op haar kind via verticale overdracht (in utero) en via contact tijdens de bevalling.
Symptomen herpetische encefalitis
De eerste tekenen van de ziekte zijn niet-specifiek en lijken op de manifestatie van veel acute infectieziekten. In het vroege stadium worden hoge temperaturen (39 °C en hoger), toenemende hoofdpijn in het voorhoofd en de slapen, zwakte, slaperigheid en verlies van eetlust opgemerkt. Misselijkheid en braken, bij ongeveer de helft van de getroffenen, voegen zich bij de symptomen van algemene intoxicatie in de eerste uren van de ziekte. Vrij snel in het vroege stadium, op de tweede of derde dag, beginnen neurologische symptomen te verschijnen, wat wijst op de mogelijkheid van herpes encefalitis.
De patiënt begint zich ongepast te gedragen en de gedragsstoornissen verergeren. Er treedt verwarring van het bewustzijn op, de patiënt verliest zijn ruimtelijk-temporele oriëntatie, herkent soms geen naasten meer, vergeet woorden en gebeurtenissen. Hallucinaties worden waargenomen - auditieve, visuele, olfactorische, tactiele, focale en zelfs gegeneraliseerde epileptische aanvallen, wat wijst op schade aan het limbisch deel van de hersenen. Gedragsstoornissen kunnen uitgesproken zijn, sommige patiënten ervaren een staat van delirium - ze zijn hyperexciteerbaar, agressief en oncontroleerbaar. In sommige gevallen (met schade aan de mediale basale gebieden van de temporaalkwabben door het virus) worden operculeuze aanvallen waargenomen - de patiënt maakt automatische kauw-, zuig- en slikbewegingen.
Herpes encefalitis bij jonge kinderen gaat vaak gepaard met myoclonische aanvallen.
Contact met een patiënt brengt al in een vroeg stadium bepaalde problemen met zich mee, zoals een vertraging van de mentale reacties, geheugenverlies, verwardheid en een verminderd bewustzijn.
Het vroege stadium van herpetische encefalitis duurt gewoonlijk enkele dagen, soms tot een week, maar kan snel evolueren en binnen enkele uren uitgroeien tot het hoogtepunt van de ziekte, dat wordt gekenmerkt door bewustzijnsstoornissen tot aan de ontwikkeling van sopor en coma. In een staat van sopor is het bewustzijn van de patiënt afwezig, reageert hij niet op aangesproken worden, maar blijven motorische reacties op pijn, licht en auditieve stimuli behouden. [ 36 ], [ 37 ]
In een reeks van 106 gevallen van HSVE waren de voornaamste redenen voor ziekenhuisopname toevallen (32%), abnormaal gedrag (23%), bewustzijnsverlies (13%) en verwardheid of desoriëntatie (13%).[ 38 ]
Symptomen die wijzen op de ontwikkeling van een coma bij een patiënt zijn onder andere stoornissen in het ademhalingsritme, met periodieke pauzes (apneu), motorische stoornissen aan beide zijden, symptomen van decorticatie (ontkoppeling van de hersenschors) en decerebratie (ontkoppeling van het voorste deel van de hersenen). Deze houdingsreacties zijn uiterst ongunstige tekenen.
De houding die het begin van decorticate rigiditeit aangeeft, is dat de bovenste ledematen gebogen zijn en de onderste ledematen gestrekt. De houding van decerebratie is dat het lichaam van de patiënt als een touw wordt opgetrokken, alle ledematen gestrekt zijn, de strekspieren gespannen zijn en de ledematen gestrekt zijn. De mate van hersenstamschade wordt bepaald door de mate van verminderd bewustzijn en disfunctie van de aangezichts- en bulbaire zenuwen.
Bij gebrek aan adequate behandeling ontwikkelt zich hersenoedeem, waarbij de locatie van de romp ten opzichte van andere structuren verschuift. Meestal raken de temporale hersengebieden ingeklemd in de tentorale opening, wat gepaard gaat met een drietal symptomen: bewustzijnsverlies, pupilafwijkingen (anisocorie) en verzwakking van een lichaamshelft. Er worden ook andere focale letsels van de hersenen en hersenzenuwen waargenomen.
De regressie van herpetische encefalitis treedt op aan het einde van de maand na het begin van de ziekte en de duur ervan kan in maanden worden berekend. Ongeveer een vijfde van de patiënten herstelt volledig, de rest heeft levenslang neurologische deficiënties van wisselende ernst. Dit kunnen lokale psychomotorische stoornissen zijn, of er kan sprake zijn van een vegetatieve toestand.
Herpetische encefalitis bij pasgeborenen wordt het meest verdragen door premature en verzwakte kinderen. Zij hebben de ziekte vaak in een fulminante necrotische vorm of ontwikkelen snel ademhalingsfalen, wat leidt tot coma. Er is meestal geen huiduitslag, maar er zijn bijna altijd stuiptrekkingen en parese, waardoor de slikreflex verstoord is en het kind niet kan eten.
Bij voldragen baby's is het beloop meestal milder. De aandoening verergert geleidelijk - hyperthermie, het kind is zwak en grillig, er is geen eetlust. Later kunnen neurologische symptomen optreden - convulsies, myoclonus, parese.
Chronische progressieve herpetische encefalitis bij pasgeborenen manifesteert zich met symptomen in de eerste of tweede levensweek. De temperatuur van de baby stijgt, hij wordt lethargisch en jengelend, er verschijnen karakteristieke blaasjes op het hoofd en lichaam, en later komen er epileptiforme symptomen bij. Zonder behandeling kan de baby in coma raken en overlijden.
Herpetische encefalitis bij volwassenen en oudere kinderen komt ook voor in verschillende mate van ernst. Het klassieke acute beloop van de ziekte, veroorzaakt door het eerste en tweede virustype, is hierboven beschreven. Subacuut wordt gekenmerkt door relatief minder uitgesproken symptomen van intoxicatie en neurologische uitval. Er is geen sprake van comateuze toestand, maar hyperthermie, hoofdpijn, fotofobie, misselijkheid, koortsstuipen, slaperigheid, cognitieve stoornissen, vergeetachtigheid en verwardheid zijn altijd aanwezig.
Daarnaast bestaan er ook "mildere" varianten van de ziekte. Chronische, trage herpetische encefalitis is een progressieve virale hersenlaesie die vooral mensen ouder dan 50 treft. De symptomen verschillen van het acute beloop door een geleidelijke toename. Een persoon merkt een constante toename van vermoeidheid en progressieve zwakte op. Zijn temperatuur kan periodiek, bijvoorbeeld 's avonds, stijgen tot subfebriele waarden, of er kan een constante subfebriele temperatuur zijn. Tegen de achtergrond van verhoogde nerveuze en fysieke stress, stress, na verkoudheid en griep, wordt in de regel een verergering van het trage proces waargenomen. De asthenie van het lichaam neemt toe en leidt uiteindelijk tot een afname van het intellectuele potentieel, verlies van werkvermogen en dementie.
Een van de vormen van trage herpetische encefalitis is het chronisch vermoeidheidssyndroom, dat meestal wordt veroorzaakt door een eerdere ziekte met griepachtige verschijnselen. Hierna kan de patiënt gedurende een lange periode (meer dan zes maanden) niet herstellen. Hij voelt zich constant zwak en is moe van de dagelijkse beslommeringen, die hij vóór de ziekte niet opmerkte. Hij wil voortdurend liggen, zijn prestaties zijn nul, zijn aandacht is verstrooid, zijn geheugen laat hem in de steek, enzovoort. De oorzaak van deze aandoening wordt momenteel beschouwd als een neurovirale infectie, en de meest waarschijnlijke etiologische factoren zijn herpesvirussen, niet alleen gewone herpes, maar ook HSV-3 en HSV-7.
Herpetische encefalitis wordt ingedeeld volgens verschillende criteria. Afhankelijk van de ernst van de symptomen (beloop) wordt de ziekte onderverdeeld in acuut, subacuut en chronisch recidiverend.
Afhankelijk van de mate van beschadiging van het hersenweefsel wordt er onderscheid gemaakt tussen een focaal en een diffuus ontstekingsproces.
De lokalisatie van de laesies wordt weerspiegeld in de volgende classificatie:
- ontsteking van voornamelijk de grijze stof in de hersenen - polio-encefalitis;
- overwegend wit - leuko-encefalitis;
Een algemeen proces dat alle weefsels aantast, is panencefalitis.
Complicaties en gevolgen
Herpetische encefalitis is een potentieel geneesbare ziekte, maar tijdige behandeling is van groot belang. Bij afwezigheid of een laat begin van de ziekte leidt de ziekte vaak tot de dood van de patiënt of tot ernstige neuropsychiatrische complicaties. Het ernstigste gevolg van herpetische encefalitis is akinetisch mutisme of een progressieve vegetatieve toestand. De patiënt verliest volledig het intellectuele vermogen, spreekt of beweegt niet, alleen de slaap-waakcyclus is volledig hersteld. Bovendien blijven de ademhaling en de bloedsomloop intact. Alle andere levensprocessen verlopen abnormaal: de patiënt kan niet eten, drinken, zijn persoonlijke hygiëne niet controleren en heeft geen controle over het legen van darmen en blaas. Deze aandoening is onomkeerbaar en is een gevolg van grootschalige schade aan hersenweefsel. Het ontwikkelt zich bij patiënten na een langdurig coma.
Veel patiënten die een ernstige vorm van herpes encefalitis hebben overleefd, lijden aan levenslange, aanhoudende neuropsychiatrische aandoeningen van wisselende ernst: hemiparese, hemiplegie, visuele en auditieve stoornissen (vaak aan één kant), epileptische aanvallen. [ 39 ]
Diagnostics herpetische encefalitis
Het idee van een dergelijke diagnose wordt vooral ingegeven door de aanwezigheid van neurologische stoornissen - ongepast gedrag, toevallen, verwardheid, die gepaard gaan met symptomen als hoge temperatuur en ernstige hoofdpijn.
Bij verdenking op herpesencefalitis worden dringend testen voorgeschreven (microscopisch onderzoek van cerebrospinaalvocht en de polymerasekettingreactie ervan om fragmenten van het herpesvirusgenotype te detecteren), evenals instrumentele studies, waarvan de meest informatieve nucleaire magnetische resonantiebeeldvorming (MRI) is. Indien dit niet mogelijk is, worden computertomografie en elektro-encefalografie uitgevoerd [ 40 ], die nuttig kunnen zijn om de effectiviteit van anti-epileptica te beoordelen. De verraderlijkheid van de ziekte is echter dat in de vroege stadia van ontwikkeling de diagnostische criteria mogelijk niet verder gaan dan de norm. Vervolgens worden de studies gedurende de eerste week herhaald.
Polymerasekettingreactie (PCR) van cerebrospinaalvocht levert zeer nauwkeurige resultaten op en maakt het mogelijk traumatisch onderzoek zoals een biopsie van hersenweefsel te vervangen. De gedetecteerde DNA-fragmenten van het herpesvirus wijzen op de herpetische oorzaak van encefalitis en het positieve resultaat van de studie blijft een week na aanvang van de antivirale therapie behouden.
Bij microscopie van de substantie van het ruggenmerg is lymfocytose te zien, de aanwezigheid van erytrocyten (in de hemorragische vorm), verhoogde eiwitniveaus en verlaagde of normale glucoseniveaus.
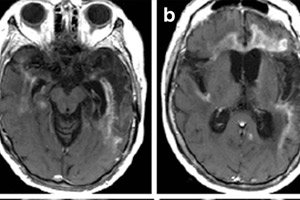
De belangrijkste beeldvormingsmethode is nucleaire MRI. Deze wordt gebruikt voor spoedindicaties. Bovendien maakt het mogelijk om te verduidelijken of de patiënt een lumbaalpunctie kan ondergaan voor analyse. Herpes encefalitis op MRI toont verhoogde signalen in de temporale kwabben of insulaire regio van de hersenschors, op het oppervlak van de orbitofrontale gyri, die worden gekenmerkt door unilaterale of bilaterale schade zonder symmetrie. Deze resultaten zijn niet specificiek, maar samen met klinische symptomen en laboratoriumgegevens maken ze in de meeste gevallen een nauwkeurige diagnose mogelijk. [ 41 ]
Vroege diagnostiek bevestigt niet altijd de diagnose: bij 10% van de patiënten zijn de CSF-microscopie en MRI-gegevens, en bij 5% zijn de PCR-resultaten vals-negatief. [ 42 ] Bij de meeste patiënten bevestigt echter ten minste enig onderzoek de diagnose, en daaropvolgende visualisaties laten duidelijke en progressieve veranderingen zien - de aanwezigheid van oedeem en bloedingen, diffuse verspreiding van de laesies.
Differentiële diagnose
In de eerste plaats is het noodzakelijk de oorsprong van de ziekteverwekker te identificeren, aangezien de belangrijkste behandeling gericht is op het neutraliseren ervan: virale encefalitis vereist een massale antivirale therapie, bacteriële encefalitis vereist antibiotica, parasitaire encefalitis vereist geschikte antiparasitaire medicijnen, enz. In deze zin spelen de resultaten van tests, met name PCR, een beslissende rol. [ 43 ], [ 44 ]
Herpetische encefalitis moet worden onderscheiden van multiple sclerose, neoplasmata, abcessen, cerebrale circulatiestoornissen, bijvoorbeeld bij een beroerte in de middelste hersenslagader zijn de basale ganglia meestal beschadigd (wat zichtbaar is op een MRI), terwijl ze bij herpetische encefalitis niet zijn aangetast, myelitis - een ontsteking van het ruggenmerg, vooral omdat gedissemineerde neuro-infectie zich vaak verspreidt naar delen van het ruggenmerg (herpetische encefalomyelitis).
Het HSV-2-virus veroorzaakt vaker een ontsteking in de zachte hersenvliezen (herpetische meningitis) dan HSV-1, hoewel deze zelden lokaal is. De ontsteking verspreidt zich snel naar de hersenmaterie – neuronen en gliacellen – en er ontwikkelt zich herpetische meningo-encefalitis. Als de oorsprong van de ziekteverwekker is vastgesteld, is het behandelprincipe vergelijkbaar (antivirale therapie). Het getroffen gebied is echter groter en de complicaties en gevolgen kunnen ernstiger zijn. Er wordt een onderscheid gemaakt op basis van de resultaten van instrumentele studies.
Met wie kun je contact opnemen?
Behandeling herpetische encefalitis
Patiënten met een vermoeden van acute hersenschade door het herpes simplex-virus worden noodzakelijkerwijs in het ziekenhuis opgenomen en op de intensive care-afdeling opgenomen. [ 45 ] Dit komt door de grote kans op het ontwikkelen van een coma, ademhalingsfalen, slikproblemen en andere vitale functiestoornissen die thuis niet in stand kunnen worden gehouden.
In de beginfase wordt aanbevolen om het antitrombotische middel Curantil driemaal daags toe te dienen in een eenmalige dosis van 25-50 mg. Dit wordt gedaan om ischemische cerebrale circulatiestoornissen te voorkomen.
De belangrijkste behandeling is etiotropisch, gericht op het verminderen van de activiteit van het herpesvirus (het is momenteel niet mogelijk om het volledig te vernietigen). Het voorkeursmedicijn is Acyclovir en de synoniemen ervan, die vooral effectief zijn tegen de herpesvirussen HSV-1 en HSV-2. Tijdige antivirale therapie kan de kans op een gunstige afloop van de ziekte en minimale complicaties vergroten.
Acyclovir is een geneesmiddel dat zich richt op zogenaamde moleculaire targets, een purine-analoog van guanine, een bestanddeel van nucleïnezuren. Een vergelijkbare structuur zorgt ervoor dat acyclovir de viruscel kan binnendringen en, in wisselwerking met de enzymen, kan omzetten in acyclovirtrifosfaat. Wanneer het in de virale DNA-keten wordt opgenomen, wordt het reproductieproces van het pathogene micro-organisme verstoord. Bovendien heeft acyclovir geen significant effect op het genetisch apparaat van menselijke cellen en bevordert het de mobilisatie van de immuniteit.
Patiënten met ernstige vormen van herpes encefalopathie met de ontwikkeling van coma krijgen aciclovir voorgeschreven in een enkele dosis van 10-15 mg per kilogram van het gewicht van de patiënt driemaal daags intraveneus. Het wordt meestal toegediend via een infuus, omdat het medicijn heel langzaam in de ader moet worden toegediend. De behandelingskuur duurt één tot twee weken. Het voordeel van aciclovir bij HSVE werd vastgesteld door twee baanbrekende klinische onderzoeken die halverwege de jaren tachtig werden uitgevoerd. Whitley et al. [ 46 ]. De huidige richtlijnen bevelen aan om aciclovir intraveneus te gebruiken gedurende 14-21 dagen in gevallen van HSV. [ 47 ]
Bij mildere vormen van de ziekte, waarbij de patiënt zelf medicijnen kan doorslikken, kan het medicijn in tabletvorm worden voorgeschreven.
Acyclovir is ook verkrijgbaar in tabletten. De dosering wordt door een arts voorgeschreven, afhankelijk van de toestand en leeftijd van de patiënt, aangezien encefalitis met hoge doses van het medicijn wordt behandeld. Bij patiënten met ernstige vormen van nierfalen wordt de dosering aangepast. Tabletten worden voor therapeutische doeleinden tot vijf keer per dag ingenomen.
Indien mogelijk wordt soms de voorkeur gegeven aan valaciclovir. Dit is een moderner medicijn met als voordeel dat het langdurig werkt en minder vaak hoeft te worden ingenomen dan zijn voorganger. In het lichaam wordt de werkzame stof afgebroken tot aciclovir, dat de belangrijkste, antiherpetische werking heeft, en valine, een alifatisch zuur, een natuurlijk bestanddeel van eiwitten. Bij herpes encefalitis is het vermogen van deze stof om de myelineschede van zenuwvezels te beschermen en te regenereren waardevol. Valine verhoogt het energiepotentieel van de spiercellen, verbetert de bewegingscoördinatie, stimuleert de celsynthese en bevordert de weefselvernieuwing.
Deze antivirale middelen zijn gecontra-indiceerd voor mensen met een overgevoeligheid voor aciclovir. Voor vitale indicaties worden ze voorgeschreven aan zwangere vrouwen, aangezien de teratogene werking van het geneesmiddel niet is vastgesteld. De volledige veiligheid is echter nog niet bewezen. Valaciclovir wordt niet voorgeschreven aan kinderen. Bijwerkingen van het gebruik ervan zijn hoofdpijn, misselijkheid, bloedvormingsstoornissen en nierfunctiestoornissen.
Uit recente onderzoeken is gebleken dat het griepmedicijn Arbidol ook werkzaam is tegen het herpes simplex-virus type 2. Naast de virale statische werking stimuleert het ook de interferonsynthese en de humorale en cellulaire immuniteit.
Andere immunomodulatoren kunnen worden voorgeschreven, zoals Laferobion (humaan interferon) of Levamisol. De dosering en duur van de inname van geneesmiddelen die het immuunsysteem stimuleren, worden door een arts voorgeschreven. Ze worden meestal gedurende een korte periode gebruikt, van drie tot vijf dagen. Ze kunnen ook allergische reacties veroorzaken en worden niet aanbevolen voor mensen met chronische hart-, vaat-, lever- en nieraandoeningen.
Om ontstekingen te verminderen en hersenoedeem te voorkomen, worden glucocorticosteroïden (Prednisolon, Medrol, Dexamethason) voorgeschreven. [ 48 ] Hun nut bij encefalitis wordt niet door alle specialisten erkend, aangezien corticosteroïden zowel een sterk ontstekingsremmend als immunosuppressief effect hebben, wat theoretisch de virale replicatie kan bevorderen. Het is niet verrassend dat er verschillende meningen zijn over hun gebruik bij HSVE [ 49 ], [ 50 ] en het aantal bijwerkingen is angstaanjagend, dus wordt pulstherapie in een korte kuur uitgevoerd. Bij het innemen ervan mogen de dosering en het regime onder geen enkele omstandigheid worden geschonden. Een niet-gerandomiseerde retrospectieve studie van 45 patiënten met HSV toonde aan dat de toevoeging van corticosteroïden aan aciclovir geassocieerd kan worden met verbeterde resultaten, [ 51 ], wat grootschaligere klinische onderzoeken aanmoedigt.
Vitamines van de B-groep worden voorgeschreven om de werking van het centrale zenuwstelsel te verbeteren, een normale stofwisseling in de hersenen te behouden en de myelineschede van zenuwvezels te herstellen. De belangrijkste voor de werking van het zenuwstelsel zijn thiamine, pyridoxine en cyanocobalamine (B1, B6, B12). Thiamine normaliseert de geleiding van zenuwimpulsen, pyridoxine versterkt de myelineschede van zenuwvezels en de productie van neurotransmitters. Cyanocobalamine vult alle bovengenoemde effecten aan en stimuleert tevens de geleiding van zenuwimpulsen naar de distale delen van het zenuwstelsel. Deze groep vitamines draagt bij aan de normalisatie van de hematopoëse, wat belangrijk is bij een dergelijke ernstige ziekte en een intensieve medicamenteuze behandeling.
Ze kunnen worden ingenomen in de vorm van tabletten (Neurorubin, Neurobion) of geïnjecteerd – elk afzonderlijk, afwisselend. Deze optie wordt als de voorkeur beschouwd.
Ook wordt ascorbinezuur toegediend. De dagelijkse dosis hiervan mag niet minder dan 1,5 gram bedragen.
Als de patiënt in een staat van psychomotorische agitatie verkeert, kunnen antipsychotica worden voorgeschreven; bij epileptische aanvallen worden ook anticonvulsiva, nootropica en bloeddrukverlagende medicijnen gebruikt.
De behandeling is symptomatisch en gericht op het stabiliseren van de werking van alle organen en systemen - dehydratatietherapie (diuretica) wordt toegepast, in ernstige gevallen - ontgifting. Vitale lichaamsfuncties worden ondersteund - ademhaling, indien nodig kunstmatige beademing van de longen; de water-elektrolytenbalans, reologische eigenschappen en samenstelling van het bloed, enz. worden genormaliseerd.
Deoxyribonuclease kan worden voorgeschreven en in geval van een secundaire bacteriële infectie een antibacteriële therapie. [ 52 ]
Vrijwel elk medicijn kan een allergische reactie bij een patiënt veroorzaken, daarom zijn desensibiliserende medicijnen (Diphenhydramine, Suprastin, Claritin) noodzakelijkerwijs opgenomen in het behandelingsregime.
Tijdens de herstelperiode kan de patiënt ook medicatie en fysiotherapie nodig hebben.
Herpetische encefalitis is een te ernstige ziekte en het is niet raadzaam om in dit geval op traditionele behandelingen te vertrouwen. De uitkomst van de ziekte hangt direct af van de snelheid waarmee met antivirale therapie wordt begonnen. Vroeger, vóór de ontdekking van antiherpetische medicijnen, lag het sterftecijfer tussen de 70 en 100%. Dus hopen op een kruidenbehandeling kan alleen maar tijd en een kans op herstel missen. Recepten met traditionele geneeswijzen kunnen echter nuttig zijn in de herstelperiode. Geneeskrachtige kruiden kunnen hoofdpijn verlichten, angst verminderen en rusteloosheid verminderen. Hartgespan, valeriaan, munt en pioenroos zijn hiervoor geschikt. Sint-janskruid staat bekend als een natuurlijk antidepressivum en echinacea is een immunomodulator. Het is echter beter om kruidenbehandelingen te gebruiken onder toezicht van een gekwalificeerde kruidkundige.
Homeopathie kan ook nuttig zijn tijdens de herstelperiode; het beschikt over veel middelen om te ontgiften, het zenuwstelsel te normaliseren en het immuunsysteem te versterken. Bij acute herpes encefalitis is het echter beter om zo snel mogelijk contact op te nemen met een specialist in infectieziekten.
Chirurgische behandeling van herpetische encefalitis wordt niet toegepast, maar als er complicaties zoals focale, medicijnresistente epilepsie optreden, kan een hersenoperatie worden aanbevolen om de oorzaak van de pathologie te elimineren. Dergelijke operaties worden uitgevoerd op basis van strikte individuele indicaties.
Het voorkomen
Het belangrijkste doel van preventieve maatregelen is het voorkomen van herpesinfecties. Dit kan worden vergeleken met pogingen om jezelf te beschermen tegen virale luchtweginfecties. Allereerst kan een goede immuniteit helpen, waarvoor een gezonde levensstijl nodig is: eet goed en gevarieerd, combineer haalbare fysieke activiteit met rust, verhoog je stressbestendigheid (want niemand kan stress in de moderne wereld volledig vermijden) en geef gewoonten op die schadelijk zijn voor de gezondheid. De praktijk leert dat het herpesvirus veel voorkomt, maar sommige mensen zijn resistent tegen infecties en hebben dit alleen te danken aan hun eigen immuunsysteem.
Als u echter iemand ziet met duidelijke symptomen van herpes labialis, mag u die persoon niet te stevig knuffelen of kussen. Als het om een familielid gaat, moet hij of zij aparte borden en hygiëneproducten gebruiken, maar deze moeten altijd individueel zijn.
Het is belangrijk om te onthouden dat de ziekte in het acute stadium ook kan worden overgedragen via druppeltjes in de lucht. Daarom is het, indien mogelijk, de moeite waard om blootgestelde lichaamsdelen die mogelijk besmet zijn met microdeeltjes van het slijm (gezicht, hals) te desinfecteren en de mond te spoelen.
Barrièreanticonceptie en het behandelen van de genitaliën met een antisepticum na contact bieden gedeeltelijke bescherming tegen genitale herpes. Maar de beste bescherming is om vrijblijvende seks te vermijden.
Als een infectie niet voorkomen kan worden, raadpleeg dan een arts en onderga regelmatig de aanbevolen antivirale therapie. U kunt uw toevlucht nemen tot traditionele geneeswijzen of een homeopaat raadplegen. Dergelijke maatregelen helpen het herpesvirus onder controle te houden en vormen een goede preventie tegen heractivering en het ontstaan van ernstige complicaties.
Prognose
Tijdige start van antivirale therapie verhoogt de kans op een gunstige prognose aanzienlijk, zelfs bij ernstige vormen van herpes encefalitis. Zonder behandeling leidt herpes encefalitis in de overgrote meerderheid van de gevallen tot overlijden of ernstige invaliditeit. Momenteel loopt een kwart tot een vijfde van de door het herpesvirus veroorzaakte ontstekingen van hersenweefsel ongunstig af. De fulminante vorm van de ziekte is bijzonder gevaarlijk en de uitbreiding van het ontstekingsproces naar de zachte hersenvliezen (meningo-encefalitis) heeft ernstigere gevolgen.
Het sterftecijfer als gevolg van onbehandelde HSV-encefalitis bedraagt ongeveer 70%, en 97% van de overlevenden zal niet terugkeren naar hun eerdere functioneringsniveau.[ 53 ],[ 54 ]
Tot de belangrijkste negatieve prognosefactoren behoren een hogere leeftijd, coma/lager bewustzijnsniveau bij presentatie, beperkte diffusie bij DWI en vertraging bij het innemen van aciclovir.
Het trage proces is gevaarlijk vanwege de lengte van de latente periode. Als gevolg hiervan zijn er, tegen de tijd dat de patiënt hulp zoekt, al uitgebreide en onomkeerbare schade aan de hersenstructuren.

